שימור פריון לגברים וילדים

שימור פריון לגברים וילדים, מיועד עבור חולים שאובחנו עם סרטן, וקיים חשש לפגיעה בפוריותם, בעקבות המחלה והטיפולים השונים. אחוזי הצלחת הטיפול וההישרדות בקרב חולי סרטן בגיל הילדות, עולים בכל שנה, בסוגים מסויימים מדובר על קרוב ל- 90% ריפוי. במציאות שכזו, רצוי לתת את הדעת על ההשלכות, ולדאוג לשימור פוטנציאל הפוריות. כאשר מדובר על גברים בוגרים ומתבגרים, ניתן להפיק בדרכים שונות זרמת זרע המכילה תאי זרע בוגרים, ולהקפיאם בבנק זרע ייעודי. בגילאי הילדות מדובר באתגר גדול יותר, מכיון שבאשכים עדיין לא מתקיים הליך ייצור תאי זרע בוגרים, והאפשרות לשימור זרע אינה קיימת. פותחו מספר אסטרטגיות טיפוליות לצורך ביצוע שימור בקרב ילדים, אך בשלב זה מדובר בהליכים ניסיוניים. הפגיעה בזרע מחקרים רבים מצביעים על כך, שבקרב מטופלים המתמודדים עם מחלת הסרטן, ישנה פגיעה בייצור הזרע, עד כדי אוליגוספרמיה חמורה (תאי זרע בודדים בזרמה), ואף אזוספרמיה (העדר תאי זרע בזרמה). בקבוצת סיכון משמעותית יותר נמצאים החולים בסרטן האשכים, או בסרטן הדם (לוקמיה, לימפומה), במיוחד מטופלים שעברו השתלת מח עצם. בקרב כ-50% מהחולים בסרטן האשכים, נצפית איכות זרע ירודה כבר משלב האבחון, עוד לפני תחילת הטיפולים. גם בקרב חולי סרטן מסוגים אחרים, תתכן איכות זרע ירודה כבר מזמן אבחון המחלה. הפגיעה בייצור הזרע עלולה להתרחש ב-4 מנגנונים: אשכים בסרטן האשכים, תאי הספרמטוגניה, שהם תאי הנבט שמהם מתפתחים תאי הזרע, עלולים להפגע ישירות מהגידול הממאיר. בשאר סוגי הסרטן, רקמות האשך עלולות להיפגע כתוצאה מהטיפולים השונים, המכילים חומרים הרעילים לאשכים (Gonadotoxic). בכלל זה עלולים להפגע תאי הספרמטוגניה, וכן תאי הסרטולי, התומכים בהליך ייצור הזרע, והם בעלי חשיבות קריטית לקיום הליך ייצור זרע (ספרמטוגנזה) תקין. לתרופות הכימותרפיות השונות, ישנה נטיה לדכא תאים המתרבים ומתחלקים במהירות – על פי רוב תאים סרטניים. בשל תכונה זו, עלולים להפגע אף תאי הספרמטוגניה, שגם להם ישנה תכונה של התרבות והתחלקות מהירה במסגרת תהליך ייצור הזרע (ראה: מילון מושגים). כמו כן, כתוצאה מטיפול ברדיותרפיה (הקרנות), במיוחד זה המכוון לאיזור המפשעה, עלולות להיפגע רקמות האשך הסמוכות לאזור ההקרנה. הורמונים בעקבות התהליך הסרטני והטיפולים היעודיים, עלולה להיפגע המערכת ההורמונלית. הציר ההורמונלי האחראי על תהליך ייצור הזרע (ספרמטוגנזה): היפותלמוס – היפופיזה (בלוטת יותרת המח) – אשכים, וההורמונים המעורבים – LH ,FSH ,GnRH, טסטוסטרון, עלול להיפגע, ויחד עימו תהליך הייצור. סרטן האשכים, מלווה בהפרשת הורמונים וחלבונים שונים (כגון – HCG ,AFP) העלולים לפגוע בתפקוד הציר ההורמונלי. ויטמינים, מינרלים ועוד לצורך ייצור הזרע הגוף זקוק לויטמינים, מינרלים, אנזימים, חומצות אמינו ופקטורים נוספים. רמתם בגוף עלולה לרדת בצורה חדה בעקבות הסרטן והטיפול האגרסיבי למיגורו. פגיעה בתאי הזרע טיפולי הכימותרפיה, עלולים לפגוע משמעותית במטען הגנטי ומבנה הDNA של תאי זרע שנוצרו לאחר תחילת הטיפול. לעיתים קרובות נצפית גם פגיעה משמעותית בתנועתיות ובמורפולוגיה. חשוב לציין, ההשפעה על תהליך ייצור הזרע תלויה במשך זמן הטיפול הכימותרפי, סוג התרופות הכימותרפיות אשר נעשה בהן שימוש ומינוני הטיפול הקרינתי. רצוי להתייעץ עם אנדרולוג מומחה, כדי לברר את מידת ההשפעה של כל טיפול על ייצור הזרע, ולבחון את ההליכים השונים לביצוע שימור פריון. שימור פריון למבוגרים ומתבגרים במטופלים בוגרים, ואף בקרב מתבגרים צעירים (בעלי אשך בנפח של לפחות 10-12 סמ"ק), ניתן להפיק פליטה של זרמת זרע טריה באמצעים שונים (פליטה לקונדום רפואי, גירוי חשמלי באמצעות ויברטור, גירוי חשמלי של חוט השדרה תחת הרדמה – EEJ). במקרים הללו, ניתן להקפיא את הדגימה בבנק זרע, גם למשך שנים ארוכות. במקרים מורכבים יותר, ניתן להפיק זרע ישירות מהאשכים או מיותרת האשך בהליך כירורגי (PESA ,MESA ,TESA ,TEFNA ,TESE ,MICRO-TESE). בקרב נערים צעירים יותר הנמצאים בתחילת גיל ההתבגרות, עשויים להימצא תאי זרע בודדים במסגרת חיפוש מעמיק במעבדה ייעודית או במסגרת הליך כירורגי. כאשר הטכנולוגיה כיום מאפשרת לבצע הפריה באמצעות הזרקת תא זרע בודד ישירות לתוך הביצית (ICSI). להליך הפקת זרע בקרב נערים בפרט, ישנן משמעויות אתיות, מוסריות, סוציאליות והלכתיות רבות. נדרשת מעורבות הורית, כדי לבחור בסוג הליך השימור הנכון וביצועו בצורה הטובה ביותר מבחינה פיזית ונפשית. יצויין כי רוב ההורים מעוניינים ומעורבים בביצוע הליך שימור פריון לבנם, מתוך תקוה להחלמתו ודאגה לעתידו. שימור פריון לילדים כאשר מדובר על ילדים, אין אפשרות לשמר תאי זרע בוגרים, כיון שעדיין לא מתקיים תהליך ייצור זרע באשכים. עם זאת הסיכונים השונים לפגיעה במערכת ייצור הזרע, קיימים במידה שווה ולעתים אף רבה יותר, בהשוואה למטופלים בוגרים. במהלך השנים האחרונות פותחו מספר אסטרטגיות טיפוליות בניסיון לבצע הליך שימור פריון לילדים. בבסיס ההליכים נעשה נסיון לשימוש ברקמת האשך הצעירה (ITT – immature testicular tissue), המכילה תאי ספרמטוגניה בלתי בשלים. רקמה זו (דגימה חלקית, ולעתים אף אשך שלם) נלקחת בביופסיה, ונחקרות דרכים שונות כדי להביא את תאי הספרמטוגניה לכדי הבשלה והפיכתם לתאי זרע בוגרים: השתלת הרקמה והחזרתה לגוף המטופל בבגרותו לצורך גידולה והבשלתה ( Autografting). השתלת הרקמה בבעלי חיים לצורך גידולה והבשלתה (Xenografting), ושאיבת תאי הזרע הבוגרים לאחר זמן לצורך הפריה. הבשלה חוץ גופית של תאי הספרמטגוניה בתנאי מעבדה (In vitro spermatogenesis), וגידולם לתאי זרע בוגרים. הליכים אלו בוצעו עד עתה בהצלחה בעכברים וקופים אך לא בבני אדם. לצורך ביצוע ההליך בפועל, נדרש פיתוח של טכניקות מתקדמות לצורך סריקת הרקמה הנלקחת, ושלילת המצאותם של תאים סרטניים בתוכה. מטופלים שלא ביצעו שימור פריון בקרב מטופלים שלא ביצעו שימור פריון, ומתקשים להגיע להריון ספונטני, עדיין קיימת האפשרות להשגת הריון. חשוב לזכור שהטכנולוגיה מאפשרת ביצוע הפריה אף אם נמצאו תאי זרע בודדים בלבד, באמצעות הזרקת תא זרע בודד ישירות לתוך הביצית (ICSI). במקרים רבים ניתן למצוא תאי זרע בקרב מטופלים שהתאוששו ממחלת הסרטן ועברו טיפולי כימותרפיה/הקרנות, בדרך דומה לטיפול בשאר סוגי האזוספרמיה – באמצעות ביצוע הליך כירורגי להפקת זרע. באזוספרמיה על רקע סרטני, מומלץ לנסות ולהפיק זרע דוקא בניתוח מיקרו-כירורגי (Micro-TESE). במסגרת הניתוח מבוצע חיפוש מדוקדק בכל אזורי אשך, ונבחרים באופן סלקטיבי חלקים מיקרוסקופיים בעלי סכוי גבוה יותר להימצאות תאי זרע (ראה: טסה או מיקרו טסה?), בכך אנו מעלים את הסיכוי להגיע לאיזורים שלא נפגעו כתוצאה מהטיפול הכימותרפי או הרדיותרפי. לעתים ניתן לחסוך את ביצוע ההליך הכירורגי, באמצעות חיפוש זרע מעמיק במעבדות מיוחדות המתמחות באיתור תאי זרע נדירים (ראה: אזוספרמיה – בירור וטיפול).[/vc_column_text][/vc_column][/vc_row]
שימור פריון

למי מיועד הליך שימור פריון? מהי מטרתו? שימור פריון מיועד לאשה המעוניינת לשמר את פוטנציאל הפוריות שלה, לפני הדרדרות צפויה ברמת הפוריות. יש להבחין בין 2 מקרים שונים: 1. שימור פריון על רקע רפואי 2. שימור פריון על רקע סוציאלי שימור פריון על רקע רפואי שימור פריון על רקע רפואי, מיועד עבור אשה אשר אובחנה עם סרטן, ועומדת לעבור טיפולי כימותרפיה/הקרנות העלולים לפגוע בפוריותה. השימור מתבצע על ידי מספר דרכים: טיפול תרופתי המפחית את מידת רגישות השחלה ופגיעותה, הקפאת ביציות/עוברים, ואף הקפאת רקמת שחלה לצורך השתלתה בעתיד. את שיטת השימור בה משתמשים, יש להתאים באופן אישי לכל מטופלת. רצוי מאד ואף הכרחי במסגרת ההליך הרפואי לטיפול בסרטן, להתייעץ עם מומחה פריון בנוגע לשימור פריון והדרכים השונות לביצוע ההליך. שימור פריון על רקע סוציאלי שימור פריון על רקע סוציאלי, מיועד עבור נשים בגילאי ה30+, המעונינות לשמר את פוטנציאל הפוריות שלהן, לפני ירידה צפויה באיכות הביציות. בדרך כלל מדובר בשימור על רקע רווקות מאוחרת, ולעתים אף בעקבות בעיית פוריות קשה אצל בן הזוג שמחמתה לא נמצאו אצלו תאי זרע (אזוספרמיה), בציפייה לפתרונות עתידיים שיאפשרו הפקת זרע מוצלחת: חיפושים/ניתוחים חוזרים, הפריה על ידי תאי זרע ראשוניים (ספרמטידים עגולים), ועוד. על פי אישור משרד הבריאות משנת 2011, כל אישה בגיל 30-41 יכולה לבצע תהליך שימור פריון מסיבות סוציאליות, כאשר החוק מאפשר לבצע עד 4 מחזורי טיפול או עד שאיבה של 20 ביציות, המוקדם מביניהם. עם זאת יצויין כי ההליך אינו נמצא בסל הבריאות, ומימונו הוא באופן פרטי, אך בחלק מקופות החולים ובחלק מבתי החולים ניתן לבצעו במחיר מוזל. מדוע חשוב לבצע שימור פריון? בניגוד לגבר, שממשיך לייצר תאי זרע במשך חייו הבוגרים, ולגיל יש השפעה מועטה יחסית על ייצור הזרע, אצל האשה, הגיל מהווה פקטור משמעותי ביותר מבחינת איכות הביציות שניתן להפיק ממנה, כאשר החל מגיל 32 מתחילה ירידה מסוימת באיכותן, אשר מתגברת החל מגיל 35. לביצוע ההליך בגיל צעיר, ישנה עדיפות הן מבחינת כמות הביציות שניתן להפיק בכל טיפול (כאשר ככל שגילה צעיר יותר, גופה מגיב טוב יותר לגירוי הורמונלי, והאפשרות להגיע למספר גבוה של ביציות במחזור טיפול בודד, גבוהה משמעותית). אך הסיבה העיקרית היא איכות הביציות: מחקרים רבים ומקיפים מצביעים על כך, שהאחוזים של ביצוע הפריה מוצלחת המסתיימת בהריון תקין, שונים מאוד בהתאם לגיל האישה, כאשר אם בגיל 30 מדובר על למעלה מ 40% סיכוי למחזור טיפול, בגיל 40 ומעלה כבר מדובר על כ 4-5% סיכוי בלבד. כמו כן ישנו סיכוי גבוה יותר להולדת ילד עם תסמונת דאון וכדומה, כאשר מדובר על ביציות של אישה מבוגרת יותר. לעובדות אלו אין שייכות לסביבה הגניקולוגית של האישה, כגון מצב הרחם שלה, אלא אך ורק לאיכות הביציות. מסיבה זו, ישנה עדיפות גדולה לביצוע הפריה על ידי ביציות של אישה צעירה, שהסיכויים להצלחת הליך IVF ללידת ילד תקין, גבוהים לאין ערוך. ניתן לומר באופן מלא וברור, שעדיף לעבוד על ביצוע הפריה עם 5 ביציות של אישה בת 30, יותר מאשר עם 20 ביציות של אישה בת 40. ביצוע ההליך ביצוע הליך שימור פריון, דומה לביצוע הליך הפריה חוץ גופית (IVF) רגיל, עד לשלב ההחזרה. המטופלת עוברת פרוטוקול טיפול במסגרתו היא נוטלת שילוב של זריקות המכילות הורמונים שונים, חלקן מיועד לגירוי השחלות להבשיל מספר גבוה של ביציות, חלקן האחר מיועד למניעת ביוץ עצמוני מוקדם טרם זמן השאיבה, ולקראת סוף ההליך הינה נוטלת זריקה נוספת לסיום הבשלת הביציות לצורך השאיבה. פרוטוקול הטיפול מותאם ספציפית עבור כל מטופלת בהתאם לפרופיל ההורמונלי שלה. בשלב הבא הביציות נשאבות תחת הרדמה, באמצעות מחט ייעודית המחוברת למשאבת ואקום ובהכוונת אולטרסאונד. מדובר בפעולה הנמשכת כ10-20 דקות, כאשר לאחריה המטופלת נשארת להתאוששות בין שעה לשעתיים. איך נשמרות הביציות? לאחר השאיבה, הביציות עוברות הקפאה מתקדמת בהליך זיגוג (ויטריפיקציה), שבו הן מוקפאות בהליך מהיר בתוך תמיסה משמרת, דבר המונע הצטברות גבישי קרח תוך-תאיים העלולים לפגוע באיכות הביצית. הביציות המוקפאות מועברות למיכל המכיל חנקן נוזלי, המשמר אותן בטמפרטורה של 196 מעלות מינוס, וניתן לאחסנן כך במשך שנים ארוכות. סיכויי השרדות הביציות לאחר הקפאה עומדים על קרוב ל 90%. מבחינה רגולטורית, ההקפאה הינה למשך 5 שנים, כאשר בתום תקופת זמן זו יש לבקש מיחידת ה IVF את המשך ההקפאה. כיצד ניגשים להליך שימור פריון? בשלב ראשון יש לקבוע פגישה עם הרופא המטפל, בפגישה זו הרופא יעבור על התיק הרפואי של האישה, ויבחן את מידת ההתאמה לביצוע ההליך. בשלב הבא, הרופא יפנה את האשה למספר רב של בדיקות מקיפות, בבדיקות נחלקות לכמה חלקים: בדיקות כלליות לבחינת תקינות המערכת הגניקולוגית (כגון בדיקת PAP). בדיקות לשלילת בעיות בריאותיות מסוימות. ביצוע פרופיל הורמונלי מלא (ביום 3-5 לווסת), לצורך התאמת פרוטוקול גירוי הורמונלי באופן מדויק לאישה המטופלת, ועוד. בדיקה נוספת שחשובה מאוד לביצוע, היא בדיקת AMH (רזרבה שחלתית), בדיקה זו ניתנת אינדיקציה למדידת פוטנציאל הפוריות של האישה. השגחה על הביציות המוקפאות אשה דתית המעונינת בהשגחה הלכתית על הביציות המוקפאות, יכולה לקבל שירותי השגחה מארגוני סיוע שונים למאותגרי פוריות, כגון מכון פועה או ארגון בוני עולם, בתיאום מראש עמם.[/vc_column_text][/vc_column][/vc_row]
טסטוסטרון
הפעם נעסוק בהורמון ה'טסטוסטרון'. טסטוסטרון – הורמון המין הגברי, בשלב הבגרות אחראי על התפתחות גופנית גברית, ולאחר מכן במשך החיים הבוגרים, הוא מהווה כ'דלק' לגבר, ותורם לבניית מסת השריר, לצפיפות העצמות, לכח הפיזי, ליכולת הקוגנטיבית, ועוד. כמו כן תומך במערכת ייצור הזרע באשכים. מחסור בטסטוסטרון עלול להתבטא בפגיעה בתפקוד הגברי, עייפות, חוסר יכולת להתרכז, עצבנות, ותופעות לוואי נוספות, מלבד פגיעה אפשרית בייצור הזרע. אזוספרמיה מלווה לעתים רבות ברמות טסטוסטרון נמוכות, בעקבות תפקוד כללי נמוך של האשך בקרב גברים אזוספרמים, או כתוצאה מפגיעה באשך עקב ניתוח. מחסור בטסטוסטרון עלול להתבטא בתופעות שונות, שניתן לחשוב שהן נובעות מדיכאון וסטרס בשל המצב הרפואי, אך במקרים רבים הגורם הוא רמות טסטוסטרון נמוכות, שניתן להעלותן בדרכים שונות ולמנוע את תופעות הלוואי. בשלב ראשון מומלץ לבדוק בבדיקת דם פשוטה את רמות הטסטוסטרון בדם (טסטוסטרון כללי + טסטוסטרון חופשי – Free Testosteron, וכן נחוצה בדיקת אסטרדיול – E2), ולאחר מכן במקרה הצורך להוועץ ברופא לגבי דרכי הטיפול השונות. המערכת ההורמונלית ראשית נעשה הכרות עם הציר ההורמונלי: היפותלמוס – היפופיזה (בלוטת יותרת המח) – אשכים ההיפותלמוס מפריש את הורמון GnRH, הורמון זה מגרה את ההיפופיזה להפריש את הורמון LH, אשר פועל על תאי הליידיג באשכים לייצר טסטוסטרון. בעקבות הגירוי מההיפותלמוס ההיפופיזה מפרישה גם את הורמון FSH, הפועל על תאי סרטולי באשכים התומכים בייצור הזרע, וכן מווסת את הפעילות באשכים לייצור טסטוסטרון (2 הורמונים אלו נקראים יחד 'גונדוטרופינים'). הפעולה של הטסטוסטרון כפולה: 1) תמיכה במערכת ייצור הזרע באשך – על כך אחראי הטסטוסטרון שבאשכים. 2) 'דלק' למערכת הפיזית והקוגנטיבית הגברית – על כך אחראי הטסטוסטרון שבדם. רמת הטסטוסטרון הנמדדת בבדיקת הדם, היא רמתו בדם בלבד, אך באשכים רמתו היא פי 50-100. הטסטוסטרון הופך במקומות שונים בגוף (רקמות שומן, אשכים, ועוד) לאסטרדיול (E2), בתהליך הנקרא 'ארומטיזציה'. כאשר בדם ישנה רמה מספקת של טסטוסטרון או של אסטרדיול, הגוף מאותת זאת ב'משוב שלילי' להיפותלמוס, שבתגובה מפחית את הפרשת הורמון GnRH, וכתגובת שרשרת מופחתת הפרשת ההורמונים LH וFSH מההיפופיזה. רמה נמוכה של טסטוסטרון נקראת במינוח הרפואי: 'היפוגונדיזם'. רמה נמוכה של טסטוסטרון עלולה להגרם ממספר סיבות: כשל בייצורו באשך (היפוגונדיזם ראשוני) חוסר/מיעוט הפרשה של הורמוני LH וFSH מההיפופיזה (היפוגונדיזם משני/ היפוגונדוטרופיק היפוגונדיזם) הדרכים להעלאתו ישנן מספר דרכים לשם העלאת רמת טסטוסטרון. נסקור אותן ונפרט את היתרונות והחסרונות שבכל אחת. לידיעתכם, מתן טסטוסטרון ישיר (הדרכים הנפוצות הן מריחת ג'ל – טסטומקס/אנדרוג'ל, או לקיחת זריקה אחת ל3 חודשים – נבידו) אינו מיועד לגברים המעוניינים לשמר את פוריותם. הסיבה לכך – כתוצאה מהטיפול להעלאת רמת טסטוסטרון, נגרם משוב שלילי המעכב את פעולת השרשרת של הגוף: היפותלמוס (GnRH) – היפופיזה (LH, FSH) – אשכים (ייצור זרע וטסטוסטרון). בעקבות ירידה ברמת הורמוני LH וFSH, מערכת ייצור הזרע אינה מתפקדת כראוי. [כאן המקום להזהיר גם מנטילת תכשירים "טבעיים" כביכול, הניתנים להעלאת רמת טסטוסטרון או לצורך צימוח זקן וכדומה, תכשירים אלו מיוצרים ללא כל פיקוח תברואתי, אין שום ידיעה מהימנה ממה הם מורכבים, והינם עלולים להכיל טסטוסטרון ישיר וכן חומרים נוספים, העלולים לפגוע בתפקוד המערכת ההורמונלית הטבעית]. הלן מספר דרכים לאיזון המערכת ההורמונלית: 1. הפחתת המשוב השלילי התרופה איקקלומין/כלומיד (Clomifene citrate) חוסמת את הקולטנים בהיפותלמוס ובהיפופיזה, ומפחיתה את המשוב השלילי המעכב הפרשת ההורמונים השונים. כתוצאה מכך ההיפופיזה ממשיכה להפריש הורמוני LH וFSH, ורמתם בדם עולה. כתגובת שרשרת עולה אף רמת הטסטוסטרון. יצויין, כי בעקבות הטיפול עולה אף רמת האסטרדיול, ועלולות להיות לכך תופעות לוואי שונות. 2. מניעת הפיכת טסטוסטרון לאסטרדיול התרופות אנסטרזול/ארימידקס ולטרזול, מעכבות את תהליך הארומטיזציה, ומונעות הפיכה של טסטוסטרון לאסטרדיול. כתוצאה מכך רמת הטסטוסטרון נשארת גבוהה יותר, ורמת האסטרדיול יורדת. יצויין, כי להורמון אסטרדיול ישנה חשיבות גבוהה לתפקוד הגברי, לבניית העצמות, ועוד, ולרמה נמוכה שלו, עלולות להיות תופעות לוואי שונות. חשוב לדעת – לעתים רבות נעשה טיפול משולב באיקקלומין + אנסטרזול/לטרזול, לצורך וויסות הורמונלי ויצירת יחס מאוזן בין טסטוסטרון לאסטרדיול. 3. זריקות הורמונים זריקות הורמונליות שונות (פרגניל, אוביטרל, ועוד) מכילות את ההורמון HCG, המהווה תחליף להורמון LH, ופועל על תאי הליידיג שבאשכים לייצר טסטוסטרון ברמה מוגברת. לסיכום – התרופות השונות (מס' 1-2) פועלות על הציר ההורמונלי: היפותלמוס – היפופיזה – אשכים, באמצעות תיעולו וויסותו. בשונה מכך בטיפול בזריקות (מס' 3), נעשית עקיפה של הציר ההורמונלי, וההורמון החלופי פועל ישירות על האשכים. חשוב לציין כי קיימים הבדלים בתגובות לדרכי הטיפול השונות, ופרוטקול הטיפול המדוייק צריך להקבע על ידי אנדוקרינולוג בעל התמחות בפריון הגבר, או על ידי מומחה לפריון הגבר (אנדרולוג) שעבר הכשרה אנדוקרינית. כתוצאה מהטיפולים השונים עלולות להגרם תופעות לוואי שונות, אך בדרך כלל הינן קלות ומזעריות בהשוואה לתועלת המופקת.[/vc_column_text][/vc_column][/vc_row]
טיפול תרופתי בפריון הגבר

הפעם נספר לכם על טיפול תרופתי שנועד לגברים הסובלים מאי פריון, כגון אזוספרמיה (העדר תאי זרע בזרמה) לא חסימתית, או אוליגוספרמיה חמורה (תאי זרע בודדים בזרמה). לפני שאתם מתחילים בקריאה, רצוי שתקראו את מילון המושגים על ייצור זרע והורמונים, שינגיש לכם את מושגי היסוד לצורך הבנת האבחון הרפואי והליך הטיפול. ייצור הזרע כפי שאתם כבר יודעים, הליך ייצור הזרע (ספרמטוגנזה) מתרחש באשכים. בכל אשך ישנן מאות אבוביות הנקראות 'אבוביות האשך' או 'אבוביות נושאות הזרע', שבתוכן מיוצר הזרע. את דפנות האבובית מרכיבים תאי סרטולי. התומכים בייצור הזרע, באמצעות 'תיווך' בין תאי הזרע המתפתחים לבין חלבונים ואנזימים שונים התורמים להתפתחות תאי הספרמטוגניה באשך לתאים בוגרים. כמו כן הם משמשים מעין שכבת מגן, ומסננים חומרים שונים העלולים לפגוע בתאי הזרע. בניית תאי סרטולי ותפקודם התקין מושפעים מהורמון FSH. מסביב לתאי הזרע באשך, בין האבוביות, נמצאים תאי ליידיג רבים, המייצרים הורמון טסטוסטרון, החשובים לתפקוד זכרי תקין, וכן אחראים לתפקוד תקין של האשך לייצר תאי זרע. תפקודם התקין של תאי ליידיג לייצור טסטוסטרון, מושפע מהורמון LH. אם נדמה את תאי הזרע לסירות קטנות המשייטות להן בים, תאי סרטולי הינם מפרצי העגינה, ותאי הליידיג וטסטוסטרון הינם היבשה שבעורף המעגנים. תאי סרטולי עוברים התרבות (Proliferation) פעמיים במהלך החיים – בשלבים האחרונים של העובר וממשיכים מיד לאחר הלידה, וכן בגיל ההתבגרות, אז הם מקבלים תכונות סופיות כדי לספק סביבה תקינה לייצור תאי הזרע. ניתן לזהות בעייה בייצור הזרע (אוליגוספרמיה חמורה או אזוספרמיה) הנובעת מכשל באשך, באמצעות בדיקה פיזית – נפח נמוך ורקמה רכה, בעקבות מיעוט תאי סרטולי, וכן בגלל שאבוביות הזרע ריקות מתאי זרע. תאי ליידיג מיוצרים בעובר אך נעלמים בגיל שנה, ומופיעים שוב בגיל ההתבגרות, אז הם עוברים התמיינות (Differentiation) ותהליך התאמה לייצור טסטוסטרון. מערכת הורמונלית ההורמונים LH וFSH, המכונים: גונדוטרופינים, מופרשים מההיפופיזה (בלוטת יותרת המח), המקבלת גירוי להפרשתם מהורמון GnRH, המופרש מההיפותלמוס. הורמון טסטוסטרון הופך במספר מקומות בגוף (רקמות שומן, אשכים, ועוד) להורמון אסטרדיול (E2) על ידי הקשרותו לאנזימים שונים, בתהליך הנקרא ארומטיזציה. האסטרדיול בעל תפקוד חשוב לבניית העצמות וכן לתפקוד מיני תקין ועוד. ערכי אסטרדיול גבוהים עלולים לגרום לתופעות לוואי שונות (כגון גינקומסטיה – גדילת שד בזכר). כאשר ישנה רמה מספקת של טסטוסטרון או אסטרדיול בדם, הגוף מאותת זאת במשוב שלילי להיפותלמוס, שבתגובה מפחית הפרשת הורמון GnRH, ובתגובת שרשרת קטנה הפרשת שאר הורמוני המין. כמו כן כאשר מתקיים ייצור זרע תקין, מופרש הורמון אינהבין B מהאשכים להיפופיזה, היוצר משוב שלילי ומעכב הפרשת הורמון FSH. חשיבות ההורמונים שיתוף פעולה של תאי סרטולי יחד עם טסטוסטרון, הוא המפתח לקיום הליך ספרמטוגנזה תקין. תהליך התפתחות תאי הזרע, החל מתאי ספרמטוגניה שהינם תאי נבט, דרך תהליכי המיטוזה והמיוזה, ועד ליצירת ספרמטיד עגול והתפתחותו לתא זרע בוגר, אינו יכול להתרחש ללא רמה תקינה של טסטוסטרון באשך. רמת הטסטוסטרון באשך גבוהה פי 50-100 מרמתו בדם, בשל חשיבותו הרבה לתפקוד מערכת ייצור הזרע. דרכי הטיפול לפני שנסביר על המקרים השונים ודרכי הטיפול הפרטניות, נתאר באופן כללי את הכלים העומדים לרשותינו כדי לנסות ולבצע איזון ברמות ההורמונים. עוד נספר לכם, כי ישנה חשיבות רבה לערכי טסטוסטרון תקינים גם לתפקוד פיזי וקוגנטיבי תקין, כאשר מחסור בטסטוסטרון עלול להתבטא בפגיעה בתפקוד המיני, עייפות, חולשה, חוסר יכולת להתרכז, עצבנות, ותופעות לוואי נוספות. כדאי שתדעו כי מתן טסטוסטרון ישיר (הדרכים הנפוצות הן מריחת ג'ל – טסטומקס/אנדרוג'ל, או לקיחת זריקה אחת ל3 חודשים – נבידו) אינו מיועד לגברים המעוניינים לשמר את פוריותם. הסיבה לכך – כתוצאה מהטיפול להעלאת רמת טסטוסטרון, נגרם משוב שלילי המעכב את פעולת השרשרת של הגוף: היפותלמוס (GnRH) – היפופיזה (LH, FSH) – אשכים (ייצור זרע וטסטוסטרון). בעקבות ירידה ברמת הורמוני LH וFSH, מערכת ייצור הזרע אינה מתפקדת כראוי. להלן מספר דרכים לאיזון המערכת ההורמונלית: 1. הפחתת המשוב השלילי התרופה איקקלומין/כלומיד (Clomifene citrate) חוסמת את הקולטנים בהיפותלמוס ובהיפופיזה, ומפחיתה את המשוב השלילי המעכב הפרשת ההורמונים השונים. כתוצאה מכך ההיפופיזה ממשיכה להפריש הורמוני LH וFSH, ורמתם בדם עולה. כתגובת שרשרת עולה אף רמת הטסטוסטרון. יצויין, כי בעקבות הטיפול עולה אף רמת האסטרדיול, ועלולות להיות לכך תופעות לוואי שונות. 2. מניעת הפיכת טסטוסטרון לאסטרדיול התרופות אנסטרזול/ארימידקס ולטרזול, מעכבות את תהליך הארומטיזציה, ומונעות הפיכה של טסטוסטרון לאסטרדיול. כתוצאה מכך רמת הטסטוסטרון נשארת גבוהה יותר, ורמת האסטרדיול יורדת. יצויין, כי להורמון אסטרדיול ישנה חשיבות גבוהה לתפקוד הגברי, לבניית העצמות, ועוד, ולרמה נמוכה שלו, עלולות להיות תופעות לוואי שונות. חשוב לדעת – לעתים רבות נעשה טיפול משולב באיקקלומין + אנסטרזול/לטרזול, לצורך וויסות הורמונלי ויצירת יחס מאוזן בין טסטוסטרון לאסטרדיול. 3. זריקות הורמונים זריקות הורמונליות שונות (פרגניל, אוביטרל, ועוד) מכילות את ההורמון HCG, המהווה תחליף להורמון LH, ופועל על תאי הליידיג שבאשכים לייצר טסטוסטרון ברמה מוגברת. זריקות אחרות (גונל F, פיוריגון, ועוד) מכילות הורמון FSH, הפועל על תאי הסרטולי באשך, ומעודד את בנייתם ותפקודם התקין. סוג נוסף של זריקות (מנוגון, מנופור, ועוד) מכיל שילוב של 2 ההורמונים. לסיכום – התרופות השונות (מס' 1-2) פועלות על הציר ההורמונלי: היפותלמוס – היפופיזה – אשכים, באמצעות תיעולו וויסותו. בשונה מכך בטיפול בזריקות השונות (מס' 3), נעשית עקיפה של הציר ההורמונלי, וההורמונים החלופיים פועלים ישירות על האשכים. חשוב לציין כי לטיפולים השונים עלולות להתלוות תופעות לוואי מסויימות, ויש לבצע את הטיפול בליווי רפואי צמוד. מקרים לטיפול ישנם מקרים שונים המתאימים לטיפול תרופתי-הורמונלי באי פריון הגבר. נבחין בין ההגדרות הרפואיות השונות: 1. היפוגונדטרופיק היפוגונדיזם (HH) הורמונים גונדטרופינים (LH וFSH) נמוכים, וכן טסטוסטרון נמוך. 2. היפוגונדיזם הורמונים גונדוטרופינים תקינים, טסטוסטרון נמוך. 3. היפרגונדטרופיק היפוגונדיזם הורמונים גונדטרופינים גבוהים, לעתים מלווה גם בהיפוגונדיזם – טסטוסטרון נמוך. היפוגונדטרופיק היפוגונדיזם (HH) כאשר ההורמונים הגונדטרופינים והטסטוסטרון נמוכים, נקודת ההנחה היא שמחסור בהפרשת ההורמונים בציר היפותלמוס – היפופיזה, הוא הגורם לחוסר פעילות תקין של מערכת הורמוני המין. דרך הטיפול תהיה על ידי החלפת הציר ההורמונלי שאינו פועל באופן סדיר, והשפעה ישירה על האשכים, באמצעות זריקות המכילות את ההורמונים HCG וFSH , במטרה להשלים לגוף את החסר ולגרום למערכת ייצור הזרע לתפקד כראוי. הורמון HCG ניתן במטרה לעודד את תאי הליידיג לייצר טסטוסטרון (מחליף את הורמון LH המופרש מההיפופיזה). והורמון FSH ניתן במטרה להבשיל את תאי הסרטולי ולהקנות להם תכונות סופיות. מדובר בטיפול ממושך יחסית עד שהגוף מגיע לפעילות תקינה, בסדר גודל של בין שנה וחצי ל-3 שנים. במהלך הטיפול מתבצע מעקב סדיר אחרי המטופל מדי מספר שבועות, במסגרתו נבדקת תגובת הגוף למתן ההורמונים, וכן מתבצעת בדיקה פיזית של האשכים, האם הינם גדלים ומתפתחים בעקבות הטיפול. עם זאת חשוב להבחין בין מספר מקרים שונים של HH, כאשר קיימים הבדלים בדרכי הטיפול וסיכויי ההצלחה:
מילון מושגים – ייצור זרע והורמונים
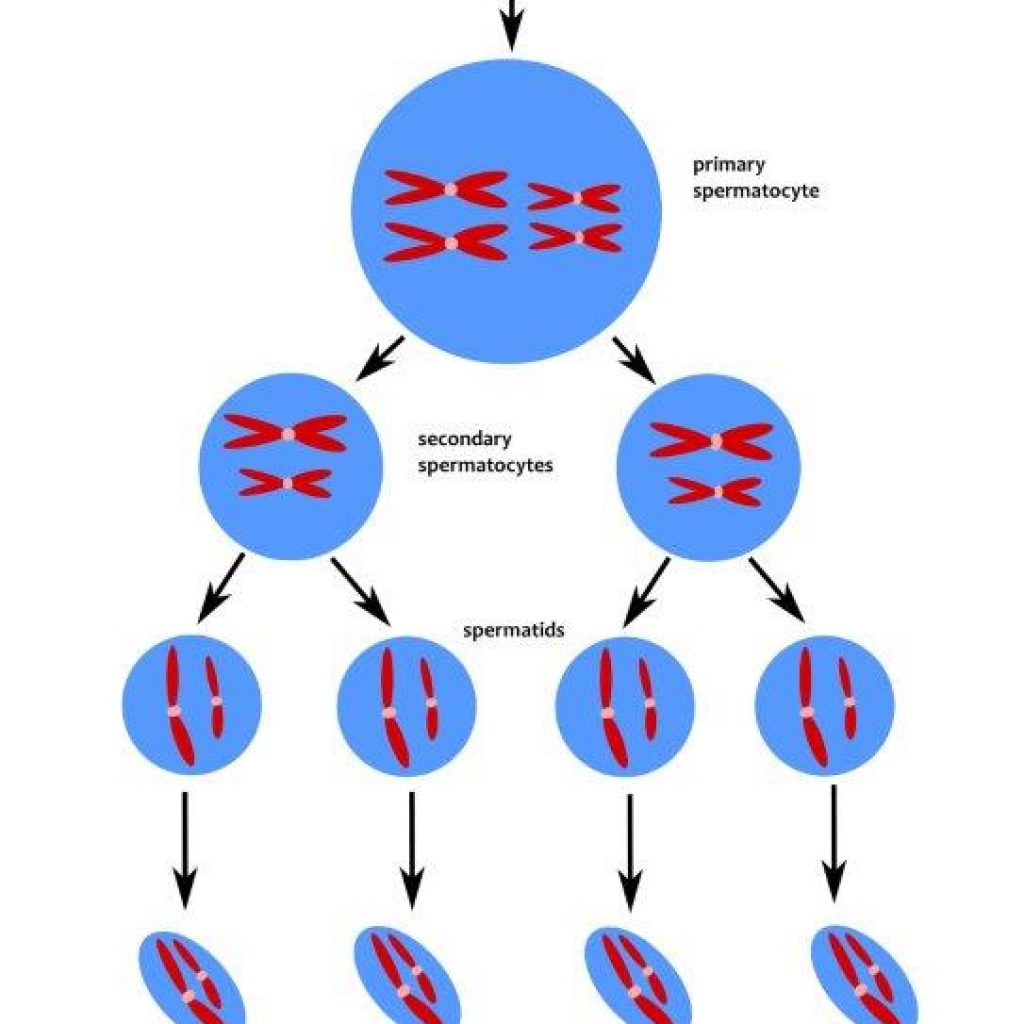
ייצור זרע אשך (Testis) – בלוטה המהווה חלק ממערכת הרבייה של הזכר, בה מתרחש ייצור הזרע וכן ייצור הורמונים שונים (טסטוסטרון ועוד). אבוביות האשך (Seminiferous tubules) – צינוריות מפותלות באשכים, בהן מתרחש תהליך ייצור הזרע (ספרמטוגנזה). ספרמטוגנזה (Spermatogenesis) – תהליך התפתחות והבשלת תאי הזרע, ראשיתו בתאי נבט (ספרמטוגוניה), העוברים מספר שלבים עד להפיכתם לתאי זרע בוגרים. הליך הספרמטוגנזה נמשך כ-60 יום. תאי הזרע הבוגרים שוהים 12-16 נוספים באפדידימיס (יותרת האשך), שם הם רוכשים את יכולת התנועתיות שלהם ותכונות נוספות. ספרמטוגוניה (Spermatogonium) – תא נבט שהינו 'תא האב' של תאי הזרע הבוגרים. בעל 46 כרומוזומים. במסגרת הספרמטוגנזה התא עובר תהליכי מיטוזה ומיוזה, שבסופם הופך ל- 4 תאי זרע. מיטוזה (Mitosis) – התהליך שבו תא מתחלק ויוצר שני תאים חדשים זהים. בתהליך ייצור הזרע, תא הספרמטוגוניה עובר מיטוזה לשני תאי ספרמטוציט ראשוני. כל תא ספרמטוציט הוא בעל 46 כרומוזומים. מיוזה (Meiosis = חלוקת הפחתה) – תהליך חלוקה המתרחש בתאי הרבייה (תאי זרע וביציות) בלבד. ספרמטוציט מתחלק ל2 תאי ספרמטיד ב2 שלבים: 1) ספרמטוציט ראשוני עובר תהליך בו סידורו הגנטי משתנה מ-46 כרומוזומים, לתא בעל 23 זוגות כרומוזומים, הנקרא ספרמטוציט שניוני. 2) כל ספרמטוציט שניוני עובר תהליך הפחתה נוסף מ-23 זוגות ל-23 כרומוזומים בודדים, בתהליך חלוקה לשני ספרמטידים. התוצר מהתא הראשוני (ספרמטוגניה) הינו ארבעה תאי ספרמטיד הפלואידיים (הפלואיד = תא בעל סט יחיד של כרומוזומים). ספרמטיד (Spermatid) – תא זרע ראשוני, בעל 23 כרומוזומים. בראשיתו עגול, ובהמשך מתפתח לתא בעל ראש וזנב. שוהה באבוביות האשך עד לסיום התפתחותו לתא זרע בוגר. הורמונים היפותלמוס (Hypothalamus) – בלוטה במח, האחראית על מספר הליכי ויסות ואיזון בגוף, וביניהם מפרישה הורמון GnRH ועוד. GnRH – הורמון משחרר גונדוטרופינים. הורמון המופרש מההיפותלמוס ואשר משפיע על היפופיזה, ומגרה אותה להפריש את ההורמונים הגונדוטרופינים. גונדוטרופינים (Gonadotropin) – ההורמונים LH וFSH. בתרגום מילולי: 'גונדות' הן בלוטות הורמוני המין (אשכים אצל הגבר, שחלות אצל האשה), ו'טרופינים' הם מזינים/ממריצים = ההורמונים המשפעלים את בלוטות המין. היפופיזה (Pituitary Gland) – בלוטה מוחית, שכתוצאה מהגירוי על ידי הורמון GnRH, מפרישה את ההורמונים הגונדוטרופינים, וכן הורמונים נוספים. LH – הורמון הפועל על תאי הליידיג באשכים לייצר טסטוסטרון. FSH – הורמון הפועל על תאי סרטולי באשכים, וכן מווסת את פעילות האשכים לייצור טסטוסטרון. תאי ליידיג (Leydig cell) – תאי אשך האחראיים על ייצור טסטוסטרון. תאי סרטולי (Sertoli cell) – תאי אשך התומכים בייצור הזרע. מרכיבים את דפנות אבוביות הזרע. טסטוסטרון (Testosterone) – הורמון המין הזכרי. בגיל ההתבגרות תורם להתפתחות הגברית, ובחיים הבוגרים אחראי על תפקוד נכון של המערכת הפיזית והקוגנטיבית הגברית, וכן תומך בייצור הזרע באשכים. רמתו באשכים היא פי 50-100 מרמתו בדם. אסטרדיול (E2) – הורמון המיוצר במספר בלוטות בגוף, וכן תוצר של טסטוסטרון. ארומטיזציה (Aromatization) – הליך הפיכת טסטוסטרון לאסטרדיול, על ידי אנזימים הקיימים במספר מקומות בגוף (רקמות שומן, אשכים, ועוד). משוב שלילי (Negative feedback) – מנגנון ויסות הורמונלי, במסגרתו רמה גבוהה של הורמון מסויים מעכבת את ייצורו. בתהליך ייצור הזרע, רמות גבוהות של טסטוסטרון/אסטרדיול, גורמות למשוב שלילי המעכב את הפרשת הורמון GnRH מההיפותלמוס, ובתגובת שרשרת להפחתת הפרשת הורמוני המין הנוספים. אינהבין B – הורמון מעכב המופרש מהאשכים ומשפיע על ההיפופיזה. כאשר מתקיים ייצור זרע תקין, גורם למשוב שלילי והפחתת הפרשת הורמון FSH. היפוגונדיזם (Hypogonadism) – מחסור בטסטוסטרון. עלול להתבטא בפגיעה בתפקוד המיני, עייפות, חוסר יכולת להתרכז, עצבנות, ותופעות לוואי נוספות, וכן לפגיעה בהליך ייצור הזרע. היפוגונדיזם ראשוני – מחסור בטסטוסטרון בעקבות כשל בייצורו באשך. היפוגונדיזם משני – מחסור בטסטוסטרון בעקבות חוסר/מיעוט הפרשת הורמוני LH וFSH מבלוטת יותרת המח. היפוגונדטרופיק היפוגונדיזם (HH) – מחסור בהורמונים גונדטרופינים (LH וFSH), וכן בטסטוסטרון. יכול להתהוות מסיבות מולדות (תסמונת קלמן ועוד), או נרכשות (גידול בהיפופיזה, חבלת ראש, ועוד). קלומיפן ציטראט (איקקלומין, כלומיד) – תרופה החוסמת את הקולטנים בהיפותלמוס ובהיפופיזה, ומונעת את המשוב השלילי הגורם להפחתת הפרשת ההורמונים השונים. אנסטרזול (ארימידקס)/לטרזול – תרופות המעכבות את תהליך הארומטיזציה, ומונעות הפיכה של טסטוסטרון לאסטרדיול. HCG – הורמון הניתן כתחליף להורמון LH, ופועל על תאי ליידיג באשכים לייצר טסטוסטרון. פרגניל, אוביטרל ועוד – זריקות שונות המכילות הורמון HCG. גונל F, פיוריגון ועוד – זריקות המכילות הורמון FSH. מנוגון, מנופור ועוד – זריקות המכילות שילוב של HCG וFSH. [/vc_column_text][/vc_column][/vc_row]
טסה או מיקרו טסה?
מטופלים רבים הסובלים מאזוספרמיה (העדר תאי זרע בזרמה), ועומדים לפני ביצוע ניתוח לצורך הפקת זרע, מתלבטים בין האופציות הכירורגיות השונות. בשורות הבאות נסקור את 2 שיטות הניתוח העיקריות: טסה (TESE), ומיקרו טסה (Micro-TESE), ונדגיש את היתרונות שיש לביצוע ניתוח בגישת המיקרו טסה המתקדמת יותר. אופן ביצוע הניתוח ראשית רצוי לדעת מהו אופן הביצוע השונה בכל גישה: בניתוח טסה, מבוצעת פתיחה מועטה של מעטפת האשך, והמנתח לוקח רקמה ממספר מוקדים בצורה רנדומלית. משך הניתוח הוא עד שעה. לעומת זאת בניתוח מיקרו טסה, פנים האשך כולו נמצא מחוץ למעטפת האשך וחשוף לעיני המנתח. באמצעות מיקרוסקופ ניתוחי ייעודי, המנתח בוחן בדקדקנות תחת הגדלה גבוהה את אבוביות האשך, ובוחר באופן סלקטיבי את אלו הנראות לו מעובות, שהינן בעלות סיכוי גבוה יותר להימצאות תאי זרע בתוכן. בעזרת מכשור מיקרו כירורגי עדין, נלקחות דגימות ממספר רב של מוקדים (15-20 בממוצע) על פני כל האשך, כך שמכל מקום נלקחת דגימה מזערית ומדויקת. בסך הכללי כמות הרקמה הנלקחת הינה פחותה משמעותית בהשוואה לכמות הנלקחת בניתוח בגישת הטסה. משך הניתוח הוא כ – 3 שעות. יתרונות המיקרו טסה כאשר אנו באים לבצע ניתוח להפקת זרע, המטרה הינה כפולה: הפקת זרע יעילה, ופגיעה מינימלית באשך. לניתוח בגישת המיקרו טסה קיימים מספר יתרונות: הפקת זרע סריקה דקדקנית של אבוביות האשך ובחירה של הטובות שבהן, ממצה באופן מקסימלי את האפשרות למציאת זרע בניתוח. ייצור הזרע ברקמת האשך עשוי להיות הטרוגני: שונה בין האשכים, וכן בין חלקים שונים באותו אשך. בניתוח מיקרו טסה בו נלקחת דגימת רקמה מכל אזור באשך, נשללת באופן כמעט ודאי האפשרות להחמצה של אזור שהינו בעל סיכוי גבוה יותר לייצור זרע. כמות הזרע המופקת בניתוח, עשויה להיות גדולה יותר בגישת המיקרו טסה, בשל בחירת הרקמה הסלקטיבית. חיפוש זרע במעבדה רקמת אשך הנלקחת בניתוח, מועברת למעבדה אמבריולוגית לצורך חיפוש ואיתור תאי זרע. במסגרת הזמן שיש במעבדה לצורך ביצוע חיפוש הזרע ברקמה, ישנו יתרון חשוב לגישת המיקרו טסה. במהלך הניתוח מועברת למעבדה רקמה סלקטיבית ומועטה יחסית. האמבריולוגים סורקים פחות חומר, והאפשרות למיצוי החיפוש וביצועו בצורה מדוקדקת בכל הרקמה, גבוהה יותר. פגיעה באשך כל ניתוח טומן בחובו פוטנציאל לפגיעה מסויימת ברקמת האשך, העלולה לבוא לידי ביטוי בירידה בייצור הטסטוסטרון ועוד. בניתוח מיקרו טסה, נלקחת כמות רקמה קטנה יותר, ופוטנציאל הפגיעה באשך נמוך באופן משמעותי. כמו כן, ברקמת האשך כלי דם רבים המזינים אותה. כאשר כלי דם אלו נפגעים, האזורים המוזנים על ידם 'מתים' והופכים לצלקתיים. כלי הדם הללו כל כך זעירים, שאין כל אפשרות לראות אותם ללא שימוש במיקרוסקופ. במהלך ניתוח מיקרו טסה, המנתח בוחן בעזרת המיקרוסקופ את הדגימה הנלקחת, ומוודא שבדרך אליה לא ייפגעו כלי הדם הזעירים המצויים בסביבתה. במהלך כל ניתוח נפגעים כלי דם קטנים כתוצאה מחיתוך וחשיפת הרקמה. על מנת לעצור את הדימום, המנתח צורב אותם במחט חשמלית ייעודית. הצריבה אמנם עוצרת את זרימת הדם, אך גם עלולה לגרום לנזק באזור הצריבה. "מחט הצריבה" בה נעשה שימוש במיקרו טסה הינה דקה ביותר, ועביה הוא כשליש מהמחט בה נעשה שימוש לצריבה בטסה הרגיל. כך שהחלק היחסי של הפגיעה הסביבתית כתוצאה מצריבה, הינו קטן באופן משמעותי.[/vc_column_text][/vc_column][/vc_row]

